Vacuna contra COVID-19 de Moderna no estará lista antes de elecciones de EE.UU.
Donald Trump ha expresado en repetidas ocasiones el deseo de obtener una vacuna antes del 3 de noviembre
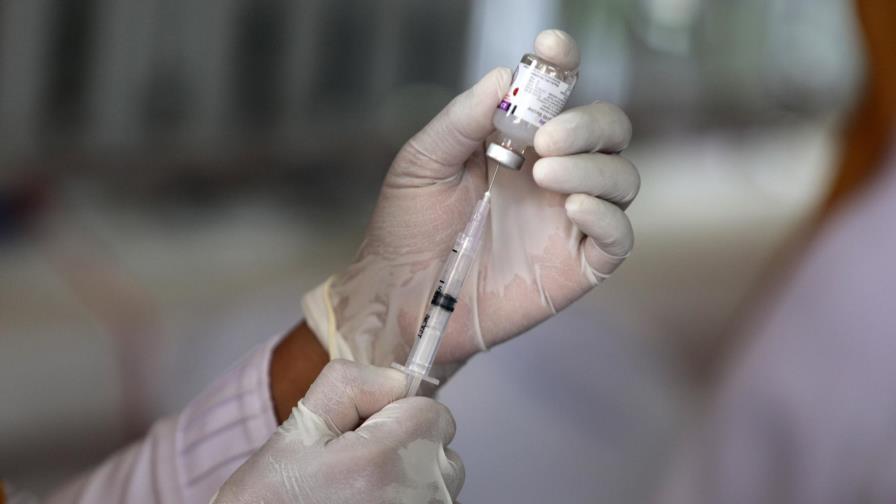
La empresa estadounidense Moderna anunció este miércoles que las pruebas clínicas de su vacuna experimental contra el COVID-19, una de las más avanzadas, no darán resultados antes del 25 de noviembre, excluyendo cualquier comercialización antes de las elecciones presidenciales en Estados Unidos.
"Tendremos suficientes datos sobre la seguridad (de la vacuna) el 25 de noviembre, para poder solicitar una aprobación de emergencia de la Agencia Federal de Medicamentos, siempre y cuando los datos de seguridad sean positivos", dijo Stéphane Bancel, director general de Moderna, en una conferencia organizada por el diario Financial Times.
Moderna, junto con las farmacéuticas estadounidenses Pfizer y Johnson & Johnson, se encuentra en la fase tres de las pruebas clínicas, en la que la vacuna experimental o un placebo se inyecta al azar en decenas de miles de voluntarios para verificar que la vacuna sea segura y eficaz.
Moderna dice que su vacuna en ciernes también genera anticuerpos en mayores
Vacuna contra el COVID-19 de Johnson & Johnson está en la última etapa de ensayos clínicos
La prueba de fase tres de la vacuna de AstraZeneca/Oxford está actualmente suspendida en el país.
El presidente estadounidense, Donald Trump, candidato a un segundo mandato, ha expresado en repetidas ocasiones el deseo de obtener una vacuna antes de las elecciones del 3 de noviembre, lo que ha suscitado la preocupación de los expertos en salud pública por la posible presión política sobre el proceso de reglamentación.
Solo un laboratorio, Pfizer, espera resultados para finales de octubre, unos días antes de la votación, lo que permitiría a la empresa solicitar inmediatamente la aprobación de la Agencia Federal de Medicamentos. Este protocolo de ensayo prevé un análisis provisional de los datos en una etapa relativamente temprana en comparación con los otros.
Pero científicos, bioestadísticos y expertos en pruebas clínicas advirtieron de los riesgos de una aprobación tan rápida, pues estiman más pertinente probar la vacuna durante unos meses más para estar seguros de su eficacia y de sus posibles efectos secundarios, especialmente porque la vacuna se administraría a cientos de millones de personas.



